Аденопросин в комплексном лечении симптомов нижних мочевых путей в сочетании с простатитом III категории
А.В. Полищук, С.В. Шкодкин, К.С. Шкодкин
ФГАОУ ВО «Белгородский государственный национальный исследовательский университет»; Россия, 308015 Белгород, ул. Победы, 85;
ОГБУЗ «Белгородская областная клиническая больница Святителя Иоасафа»; Россия, 308007 Белгород, ул. Некрасова, 8/9
Введение.
Проблема эффективной и безопасной терапии пациентов с доброкачественной гиперплазией предстательной железы (ДГПЖ) и простатитом категории III остается актуальной, несмотря на широкий спектр применяемых препаратов разных групп. В этих условиях продолжается поиск новых фармакологических средств.
Цель исследования – оценить эффективность Аденопросина в терапии симптомов нижних мочевых путей и эректильной дисфункции у пациентов с синдромом хронической тазовой боли (СХТБ) на фоне ДГПЖ.
Материалы и методы.
В исследование продолжительностью 90 дней были включены 60 пациентов в возрасте от 40 до 60 лет с СХТБ и эректильной дисфункцией на фоне ДГПЖ. Пациенты основной группы в течение 30 дней получали альфа‑1‑адреноблокатор тамсулозин в комбинации с нестероидным противовоспалительным препаратом нимесулид (в течение 5 дней) и суппозиториями Аденопросин. Пациенты контрольной группы принимали тамсулозин в течение 30 дней и нимесулид – 5 дней. В последующие 60 дней оценивалась динамика на основании данных анкет NIH‑CPSI (Шкала симптомов хронического простатита и синдрома тазовых болей у мужчин), IPSS (Международный индекс симптомов при заболеваниях предстательной железы), QoL (Шкала качества жизни), AMS (Опросник возрастных симптомов андрогенного дефицита у мужчин), МИЭФ‑5 (Международный индекс эректильной функции); анализа дневника мочеиспускания; общего анализа мочи; анализа крови на уровень простатического специфического антигена, глюкозы; анализа секрета предстательной железы; трансректального ультразвукового исследования предстательной железы с измерением остаточной мочи; урофлоуметрии.
Результаты.
Частота мочеиспусканий снизилась к 30‑м суткам в основной группе с 12,7 ± 1,4 до 7,3 ± 1,8 микций в сутки, в контрольной – с 13,1 ± 1,8 до 9,6 ± 1,1; в дальнейшем (на 60‑е и 90‑е сутки) в основной группе отмечалось сохранение положительного эффекта, а в контрольной – учащение микций. По опроснику NIH‑CPSI отмечено уменьшение выраженности симптоматики к 30‑м суткам: в основной группе – с 25,4 ± 2,1 до 12,3 ± 1,9 балла, в контрольной – с 24,3 ± 1,7 до 17,6 ± 0,4 балла, в основной группе сохранилась тенденция к снижению выраженности симптомов, в контрольной группе отмечено усиление симптоматики к 90‑м суткам. Оценка по IPSS к 30‑м суткам снизилась в основной группе с 12,9 ± 0,5 до 5,2 ± 1,4 балла, в контрольной – с 14,1 ± 0,7 до 8,2 ± 0,9 балла; наблюдалось дальнейшее снижение показателя к 60‑м суткам в обеих группах и увеличение – к 90‑м суткам (более выраженное в контрольной группе). Качество жизни (QoL) в обеих группах улучшилось к 30‑м суткам (в основной группе – 1,4 ± 0,6 балла, в контрольной – 3,1 ± 0,8). Наблюдалось улучшение эректильной функции по данным опросника МИЭФ‑5: в основной группе с 11,5 ± 1,1 до 18,9 ± 1,4 балла к 30‑м суткам с дальнейшим сохранением тенденции, а в контрольной – с 10,7 ± 1,4 до 15,3 ± 1,1 балла с отрицательной динамикой в дальнейшем. По данным урофлоуметрии выявлена положительная динамика показателя Qmax к концу лечения в основной (с 8,3 ± 1,5 до 14,7 ± 1,1 мл/с) и контрольной (с 8,8 ± 1,3 до 13,1 ± 1,6 мл/с) группах с его снижением в дальнейшем. Объем предстательной железы в основной группе к 90‑м суткам в среднем составил 33,5 ± 3,1 см3 (при исходном объеме 42,6 ± 2,5 см3), в контрольной – 41,6 ± 1,9 см3 (при исходном объеме 43,1±1,4 см3). На фоне лечения в группах не отмечено выраженных изменений в анализах мочи, секрета предстательной железы, уровнях простатического специфического антигена и глюкозы крови.
Выводы.
По результатам исследования можно сделать вывод, что применение тамсулозина в комбинации с Аденопросином у пациентов с ДГПЖ и простатитом категории III имеет преимущество перед применением только альфа‑1‑адреноблокаторов.
Ключевые слова:
гиперплазия предстательной железы, Аденопросин, синдром хронической тазовой боли, эректильная дисфункция, симптомы нижних мочевых путей, альфа‑1‑адреноблокаторы, исследование эффективности
Введение
В настоящее время неоспоримым фактором прогрессии доброкачественной гиперплазии предстательной железы (ДГПЖ) признано наличие воспалительного компонента в предстательной железе [1]. Усиление доброкачественной простатической обструкции у этой группы пациентов зачастую сочетается с болевым простатическим синдромом как проявлением синдрома хронической тазовой боли (СХТБ) [2]. Это существенно нарушает качество жизни, так как частота и продолжительность рецидивов данного состояния усугубляют не только физическое, но и психологическое здоровье пациентов [3]. В современной классификации простатита инфекционная этиология не является единственной [4]. Примерно у 95 % больных выявляется простатит категории III, при котором отсутствует инфекционный агент и, соответственно, применение антибактериальных препаратов неэффективно [5, 6]. Данной категории пациентов проводится преимущественно симптоматическое лечение. Наиболее эффективными и часто применяемыми группами препаратов являются альфа-адреноблокаторы и нестероидные противовоспалительные препараты (НПВП), а также их комбинации [7]. Эффективность НПВП в лечении СХТБ достигала 80 % по сравнению с плацебо и приводила к улучшению качества жизни и показателя NIH-CPSI (National Institutes Health Chronic Prostatitis Symptom Index, шкала симптомов хронического простатита и синдрома тазовых болей у мужчин) [8–11]. У пациентов достоверно уменьшаются болевой синдром, дизурия, отмечается улучшение эректильной функции. Однако применение данной группы препаратов сопровождается развитием грозных осложнений, требующих ограниченного их назначения или даже отмены. В этих условиях увеличивается актуальность поиска новых фармакологических средств, обладающих анальгезирующей и противовоспалительной активностью при меньшем проявлении побочных реакций или их полном отсутствии. Препарат Аденопросин обладает схожим патогенетическим эффектом с НПВП [12]. Активные компоненты препарата уменьшают образование А2-фосфолипазы и высвобождение арахидоновой кислоты, что в свою очередь способствует снижению синтеза простагландинов и лейкотриенов. Таким образом, это способствует уменьшению проницаемости капилляров, уменьшению отека и улучшению микроциркуляции предстательной железы на фоне анальгезирующего и антиоксидантного эффектов [13].
Цель исследования – оценить эффективность Аденопросина в терапии симптомов нижних мочевых путей (СНМП) и эректильной дисфункции у пациентов с СХТБ на фоне ДГПЖ.
Материалы и методы
В исследование были включены 60 пациентов. Критерии включения: подписание информированного согласия на участие в исследовании; возраст – 40–60 лет, объем предстательной железы – до 50 см3; объем остаточной мочи – менее 50 мл; максимальный поток по урофлоурограмме – более 10 мл / с; показатель IPSS (International Prostate Symptom Score, международный индекс симптомов при заболеваниях предстательной железы) – 7–25 баллов; уровень простатического специфического антигена (ПСА) – менее 4 нг / мл.
Пациенты были распределены на 2 группы: основная группа – пациенты, принимающие альфа-1-адреноблокатор тамсулозин 0,4 мг / сут в течение 1 мес, НПВП нимесулид 100 мг / сут в течение 5 дней в комбинации с суппозиториями Аденопросин 150 мг / cут в течение 1 мес; контрольная группа – пациенты, которые принимали только альфа-1-адреноблокатор тамсулозин 4 мг / сут – 1 мес и НПВП нимесулид 100 мг / cут – 5 дней. В последующие 60 дней (по окончании курса терапии) проводилось наблюдение пациентов обеих групп для оценки эффективности лечения.
В визит включения, а также в последующие визиты были проведены следующие исследования: анкетирование по опросникам NIH-CPSI, IPSS, QoL (Quality of Life, шкала качества жизни), AMS (Aging Male Symptoms, опросник возрастных симптомов андрогенного дефицита у мужчин), МИЭФ-5 (международный индекс эректильной функции); анализ дневника мочеиспускания; общий анализ мочи; анализ крови на ПСА, глюкозу; анализ секрета предстательной железы, трансректальное ультразвуковое исследование предстательной железы с измерением остаточной мочи, урофлоуметрия. Достоверность различий оценивали с помощью непараметрического критерия Манна–Уитни, статистически значимыми считали различия при p <0,05.
Результаты
По результатам интерпретации дневников мочеиспускания отмечено уменьшение частоты мочеиспусканий в обеих группах к 30-м суткам: в основной группе – с 12,7 ± 1,4 до 7,3 ± 1,8 микций в сутки, в контрольной – с 13,1 ± 1,8 до 9,6 ± 1,1. В дальнейшем у пациентов, принимавших комбинированную терапию тамсулозин + Аденопросин и НПВП в течение 5 дней, к 60-м и 90-м суткам отмечалось сохранение положительного эффекта: соответственно 6,9 ± 1,2 и 7,6 ± 1,4 микций в сутки, а у пациентов, получавших только тамсулозин, в долгосрочной перспективе прослеживалось учащение микций: на 60-е сутки – 10,5 ± 0,4 и на 90-е сутки – 11,9 ± 1,1 (р <0,05) (рис. 1).
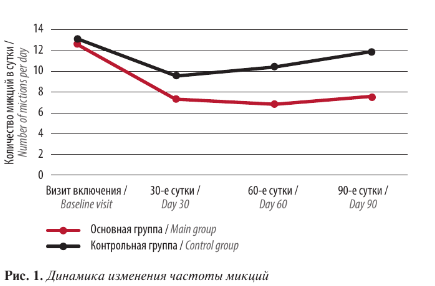
При анализе опросников NIH-CPSI до начала терапии сумма доменов в группах была более 19 баллов, что характеризует тяжелые симптомы: в основной группе – 25,4 ± 2,1 балла, в контрольной – 24,3 ± 1,7 балла (р >0,05). На 1-м визите (на 30-е сутки лечения) в обеих группах зафиксировано уменьшение симптоматики до средне-выраженных симптомов, при этом отмечались достоверные различия в группах: в основной группе средний балл составил 12,3 ± 1,9, а в контрольной – 17,6 ± 0,4 (р <0,05). Cтоит особо отметить дальнейшее уменьшение симптомов в доменах в последующие визиты: на 60-е сутки средняя сумма баллов в группе, получавшей терапию Аденопросином, составила 8,5 ± 1,4 (соответствует незначительно выраженным симптомам по шкале NIH-CPSI), а в контрольной группе – 15,3 ± 1,8 (р <0,05); на 90-е сутки в контрольной группе было отмечено усиление симптомов, сумма баллов составила 18,1 ± 2,3, при этом в основной группе нарастания симптоматики не отмечалось – 6,9 ± 1,7 балла (р <0,05) (рис. 2)
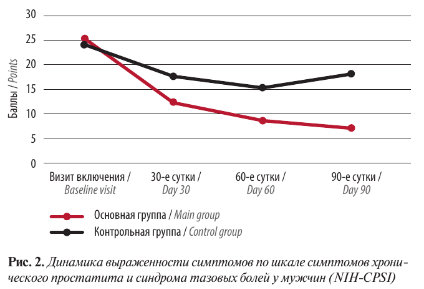
Уменьшение симптоматики в отдаленном периоде мы можем объяснить наличием стойкого противовоспалительного и анальгезирующего эффекта Аденопросина. Достоверные различия зафиксированы по другим опросникам: средняя оценка по IPSS в основной группе к 30-м суткам снизилась с 12,9 ± 0,5 до 5,2 ± 1,4 балла, в контрольной – с 14,1 ± 0,7 до 8,2 ± 0,9 балла, что характеризовало умеренную симптоматику. В основной группе на 60-е сутки оценка по IPSS составила 4,8 ± 0,3 балла и на 90-е сутки – 6,1 ± 0,5 балла. В контрольной группе также отмечалась положительная динамика на 60-е сутки – 7,6 ± 0,7 балла, с увеличением к 90-м суткам до 9,4 ± 0,3 балла (р <0,05) (рис. 3). Качество жизни также существенно улучшилось к 30-м суткам: средний балл по шкале QoL в основной группе составил 1,4 ± 0,6, в контрольной – 3,1 ± 0,8, однако к 90-м суткам пациенты контрольной группы отмечали возвращение симптомов.
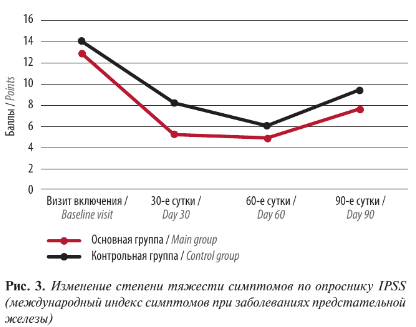
Аналогичную динамику можно проследить и в других исследованиях [14].При анализе анкет МИЭФ-5 получены следующие данные: в основной группе к 30-м суткам значение показателя выросло с 11,5 ± 1,1 до 18,9 ± 1,4 балла, тенденция к увеличению сохранялась к 60-м (20,1 ± 0,6 балла) и к 90-м суткам (21,4 ± 0,4 балла), тогда как во 2-й группе при улучшении эректильной функции к 30-м суткам (с 10,7 ± 1,4 до 15,3 ± 1,1 балла) отмечалась отрицательная динамика к 60-м (13,7 ± 0,7 балла) и 90-м суткам (11,3 ± 0,3 балла) (р <0,05) (рис. 4).
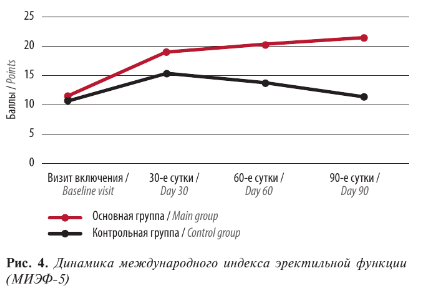
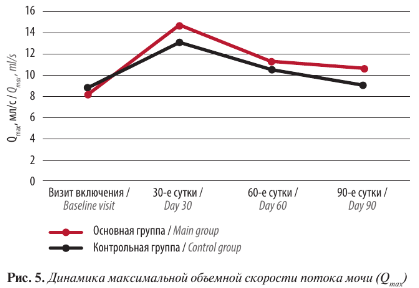
Различия в полученных результатах прослеживаются и при инструментальных методах исследования. По данным анализа урофлоуметрии, положительная динамика максимального потока к 1-му визиту отмечалась в обеих группах. У пациентов основной группы максимальная объемная скорость потока (Qmax) увеличилась с 8,3 ± 1,5 до 14,7 ± 1,1 мл / с, при этом прекращение приема тамсулозина привело к ослаблению потока Q на 60-е сутки (11,3 ± 0,8 мл / с) и 90-е сутки max (10,8 ± 0,4 мл / с), не достигнув исходных показателей (до лечения). В контрольной группе положительная динамика была не столь долгосрочной и выраженной: с 8,8 ± 1,3 до 13,1 ± 1,6 мл / с на 30-е сутки, до 10,6 ± 0,2 мл / с на 60-е сутки и 9,2 ± 0,8 мл / с на 90-е сутки (р <0,05) (рис. 5).
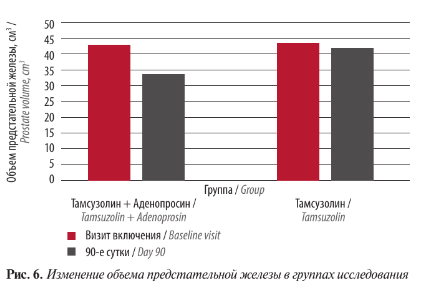
По результатам трансректального ультразвукового исследования предстательной железы отмечалось достоверное уменьшение ее объема у пациентов, получавших комбинированную терапию тамсулозин + Аденопросин. В основной группе объем предстательной железы к 90-м суткам составил 33,5 ± 3,1 см3, что меньше исходного – 42,6 ± 2,5 см3. При этом прием только тамсулозина значимо не повлиял на размер предстательной железы, который составил 41,6 ± 1,9 см3 при исходном среднем объеме 43,1 ± 1,4 см3 (р <0,05) (рис. 6).
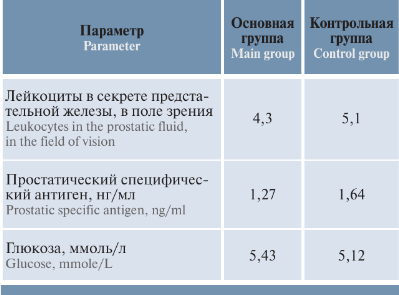
В ряде публикаций на данную тему прослеживаются схожие результаты исследований [15], что можно объяснить антиоксидантным и противоотечным действием препарата Аденопросин. На фоне лечения в группах не отмечено выраженных изменений в анализе мочи, анализе секрета предстательной железы, уровнях ПСА и глюкозы крови (р <0,05) (см. таблицу)
Выводы
Проведенное исследование позволяет сделать вывод, что комплексное применение тамсулозина и Аденопросина у пациентов с ДГПЖ и простатитом категории III имеет преимущество по сравнению с применением только альфа-1-адреноблокаторов как в кратковременной, так и в долгосрочной перспективе. Использование данного энтомологического препарата способствует снижению общего балла доменов простатических симптомов шкалы NIH-CPSI, уменьшению частоты микций, улучшению эректильной функции, а также достоверному уменьшению объема гиперплазированной предстательной железы, что значительно улучшает качество жизни пациентов.
Вклад авторов
А.В. Полищук: обзор публикаций по теме статьи, написание текста статьи;
С.В. Шкодкин: научное редактирование текста статьи, обзор публикаций по теме статьи;
К.С. Шкодкин: обработка данных литературы.
ORCID авторов
А.В. Полищук: https://orcid.org/0000-0001-5164-7128;
С.В. Шкодкин: https://orcid.org/0000-0003-2495-5760;
К.С. Шкодкин: https://orcid.org/0000-0003-4270-165X
Конфликт интересов.
Авторы заявляют об отсутствии конфликта интересов.
Финансирование.
Работа выполнена без спонсорской поддержки.
Соблюдение прав пациентов.
Все пациенты подписали информированное согласие на участие в исследовании.
Оценка эффективности применения энтомологического препарата «Аденопросин®» в комбинированной терапии пациентов с симптомами нижних мочевых путей, обусловленных доброкачественным увеличением предстательной железы
Читать дальшеОценка эффективности препарата Аденопросин у пациентов с хроническим простатитом
Читать дальшеЭффективность и безопасность Аденопросина при хроническом рецидивирующем бактериальном простатите с множественной устойчивостью уропатогенов, выделенных из секрета предстательной железы, к антибактериальным препаратам
Читать дальшеЭнтомологический препарат Аденопросин в лечении пациентов с доброкачественной гиперплазией предстательной железы и хроническим простатитом
Читать дальшеЭффективность применения препарата Аденопросин в комплексном лечении пациентов с хроническим бактериальным простатитом
Читать дальшеПрименение препарата Аденопросин у больных хроническим абактериальным простатитом
Читать дальшеЭнтомотерапия – новый тренд в урологии
Читать дальшеОценка отдаленных результатов применения энтомологического препарата в комплексной терапии пациентов с доброкачественной гиперплазией предстательной железы и хроническим простатитом
Читать дальшеОценка эффективности и безопасности препарата Аденопросин® у пациентов с хроническим простатитом IIIA категории
Читать дальшеСписок
литературы
2. Magri V., Boltri M., Cai T. et al. Multidisciplinary approach to prostatitis. Arch Ital Urol Androl 2019;90(4):227– 48. DOI: 10.4081/aiua.2018.4.227.
3. Shoskes D.A., Vij S.C., Shoskes A. et al. Development of a Clinically Relevant Men's Health Phenotype and Correlation of Systemic and Urologic Conditions. Urology 2018;114:77–82. DOI: 10.1016/j.urology.2017.12.035.
4. Клинические рекомендации Европейской ассоциации урологов 2019 г. Пер. с англ. М., 2019. 300 с. [European Association of Urologists Guidelines. Moscow, 2019. 300 p. (In Russ.)].
5. Сивков А.В. Диагностика и лечение доброкачественной гиперплазии предстательной железы. Consilium Medicum 2003;05(1):9–18. [Sivkov A.V. Diagnosis and treatment of benign prostatic hyperplasia. Consilium Medicum 2003;05(1):9–18. (In Russ.)].
6. Oesterling J.E. The origin and development of benign prostatic hyperplasia. An age-dependent process. J Androl 1991;12:348–55.
7. Урология. Российские клинические рекомендации. Под ред. Ю.Г. Аляева, П.В. Глыбочко, Д.Ю. Пушкаря. М.: ГЭОТАР-Медиа, 2018. 480 с. [Urology. Russian Clinical Guidelines. Ed. by Yu.G. Alyaev, P.V. Glybochko, D.Yu. Pushkar’. Moscow: GEOTAR-Media, 2018. 480 p. (In Russ.)].
8. Nicel J.C., Pontari M., Moon T. et al. A randomized, placebo controlled, multicenter study to evaluate the safety and efficacy of rofecoxib in the treatment of chronic nonbacterial prostatitis. J Urol 2003;169(4):1401–5. DOI: 10.1097/01. ju.0000054983.45096.16.
9. Zhao W.P., Zhang Z.G., Li X.D. et al. Celecoxib reduces symptoms in men with difficult chronic pelvic pain syndrome (Category IIIA). Braz J Med Biol Res 2009;42(10):963–7. DOI: 10.1590/s0100-879x2009005000021.
10. Chen Y., Wu X., Liu J. et al. Effects of a 6-month course of tamsulosin for chronic prostatitis/chronic pelvic pain syndrome: a multicenter, randomized trial. World J Urol 2011;29(3):381–5. DOI: 10.1007/s00345-010-0537-3.
11. Nickel J.C., Downey J., Pontari M.A. et al. A randomized placebo-controlled multicentre study to evaluate the safety and efficacy of finasteride for male chronic pelvic pain syndrome (category IIIA chronic nonbacterial prostatitis). BJU Int 2004;93(7):991–5. DOI: 10.1111/j.1464-410X.2003.04766.x.
12. Официальная инструкция по применению препарата Аденопросин. Доступно по: https://www.rlsnet.ru/ tn_index_id_96429.htm. [Official package insert for the Adenoprosin. Available at: https://www.rlsnet.ru/ tn_index_id_96429.htm. (In Russ.)].
13. Медведев В.Л., Ефремов М.Е. Эффективность применения препарата аденопросин® в комплексном лечении пациентов с хроническим бактериальным простатитом. Инновационная медицина Кубани 2020;3(19):45–51. [Medvedev V.L., Efremov M.E. The effectiveness of the use of the drug adenoprosin® in the complex treatment of patients with chronic bacterial prostatitis. Innovatsionnaya meditsina Kubani = Innovative medicine of Kuban 2020;3(19):45–51. (In Russ.)]. DOI: 10.35401/2500-0268-2020-19-3-45-51.
14. Кузьменко А.В., Кузьменко В.В., Гяургиев Т.А. Энтомологический препарат аденопросин в лечении пациентов с доброкачественной гиперплазией предстательной железы и хроническим простатитом. Урология 2021;1:39–44. [Kuzmenko A.V., Kuzmenko V.V., Gyaurgiev T.A. Entomological drug adenoprosin in the treatment of patients with benign prostatic hyperplasia and chronic prostatitis. Urologiya = Journal of Urology 2021;1:39–44. (In Russ.)]. DOI: 10.18565/urology.2021.1.39-44.
15. Dumbraveanu I., Ciuhrii C., Tanase A. Anti-inflammatory activity of Adenoprosin in nonbacterial prostatitis. The Moldovan Medical Journal 2017;60(4):3–10.
